|
|
| 血管新生の制御に関する研究 |
| 加齢医学研究所・腫瘍循環研究分野 教授 佐藤靖史 |
|
血管は、生体の基本的な構造物であり、幹細胞である血球血管芽細胞や血管芽細胞が血管内皮細胞へと分化して原始血管叢を形成する“vasculogenesis”と、血管内皮細胞が発芽や嵌入によって血管の数を増す“angiogenesis”の2つのプロセスを経て全身へと分布し、壁細胞に取り囲まれて成熟した構造物となる。成熟個体において、血管新生は本来生理的な現象であり、子宮内膜など限られた場所で一過性に見られるが、癌、糖尿病性網膜症、関節リウマチなどでは持続し、それぞれの病態の進展と密接に関連していることから、病的な血管新生の効果的な制御法の開発が期待されている。また、虚血性疾患においては、血管新生を誘導して虚血を解除する治療法の臨床導入が進められている。我が研究室では、血管新生を人為的に制御のための基盤研究を行っている。主な研究成果は以下の通りである。(1)血管新生の過程で血管内皮細胞に発現する複数の転写因子の機能を解析し、なかでも転写因子ETS-1は血管新生を促進する多機能の重要な転写因子であること、
ETS-1の標的分子を同定するとともに、血管新生を制御するための分子標的となることを示した。(2)マウス胚性幹(ES)細胞が血管内皮細胞へと分化する過程で発現する遺伝子群をスクリーニングし、その中から血管新生を促進する機能性分子としてpuromycin-insentitive
leucil-specific aminopeptidase (PILSAP)を同定した。PILSAPは、血管内皮の細胞内において、PDK1を基質とし、その翻訳後修飾によって細胞内シグナル伝達系を調節するユニークな機能をもっており、PILSAPもまた、血管新生を制御するための分子標的となることを明らかにした。(3)VEGF刺激によって血管内皮細胞に誘導される遺伝子の網羅的解析から、血管内皮細胞が産生する新規の血管新生抑制因子を見出した。本分子は、血管新生の刺激に反応して血管内皮細胞が産生・分泌し、血管内皮細胞に選択的に作用して血管新生を抑制するnegative
feedback調節因子としての特徴を持つことが示された、世界初の分子である。我々は、血管(vasculature)と抑制(inhibition)の2つの言葉を融合させ、本分子をvasohibinと命名した。現在、vasohibinの作用発現のメカニズム、各種病態における意義、診断や治療への応用、などについて研究を進めている。
|
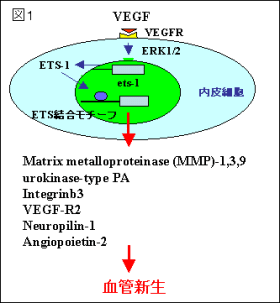 |
図1:血管内皮細胞はVEGFで刺激されると、ERK1/2のシグナルを介して早期に転写因子ETS-1を発現する。ETS-1はMMPなど複数の標的遺伝子を誘導して血管新生を促進的に調節する中心的な転写因子であり、その機能を阻害すると、血管新生は抑制される。
|
|
|
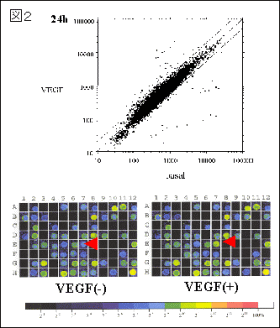 |
図2:血管内皮細胞をVEGF刺激し、発現変動する遺伝子群をcDNA microarrayで解析、刺激後24時間で2倍以上に誘導される遺伝子(赤矢印)産物の機能解析から新規の血管新生抑制因子を同定した。
|
|
|
|
|
