- TOP
- 公開情報
- 非公開: 倫理委員会名簿・議事要録
- 医学系研究に関する倫理申請について(申請手順、倫理指針、内規など)
医学系研究に関する倫理申請について(申請手順、倫理指針、内規など)
東北大学大学院医学系研究科、病院及び加齢医学研究所における医学系研究の倫理審査は、東北大学大学院医学系研究科倫理委員会(旧第1倫理委員会)及び東北大学病院臨床研究倫理委員会(旧第2倫理委員会)において行います。
歯学研究科、東北メディカル・メガバンク機構所属の研究者が行う医学系研究のうち患者介入を行う課題の審査は病院臨床研究倫理委員会において行います。
倫理委員会は、ヒトを対象とした医学系研究について、医の倫理に関するヘルシンキ宣言の趣旨に基づいて、被験者の人間としての尊厳、人権の尊重その他の倫理的・科学的観点から調査審議するために、医学系研究科長及び病院長が設置した合議制の委員会です。
倫理委員会への申請手続きの流れ
倫理申請専用のwebシステム「倫理審査申請システム」から研究を申請し、その後の必要な手続を行って下さい。
申請手続きの流れは以下の通りです。
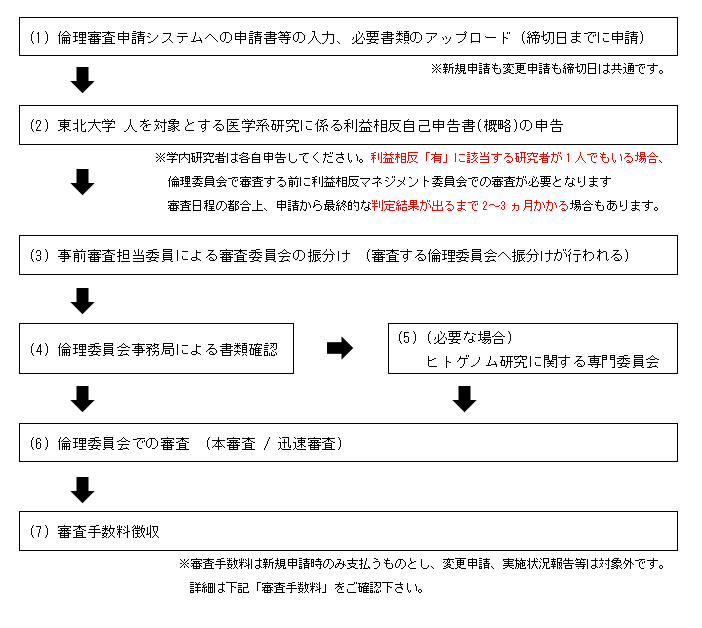
倫理審査手数料
医学系研究科倫理委員会では、東北大学大学院医学系研究科倫理委員会内規に基づき新規申請時に審査手数料を徴収します。変更申請や実施状況報告等は課金対象外です。新規申請時には申請書類とあわせて「審査手数料確認シート」を作成していただき、倫理委員会の審査後にこの書類を用いて審査手数料を徴収します。審査手数料の金額等詳細は、東北大学大学院医学系研究科倫理委員会内規および審査手数料確認シート記入要領等にてご確認下さい。(審査手数料確認シートは、下記関連リンクの「医学系研究に関する様式のダウンロード」のページでダウンロードできます。)
倫理委員会の所掌
倫理委員会は、医学系研究科倫理委員会及び病院臨床研究倫理委員会があります。両委員会の所掌は以下の通りです。(変更申請は、原則当該審査を行った委員会において審査します)
ただし、両委員長の判断で審査する委員会が変更される場合があります。
-
医学系研究科倫理委員会
【原則】
「東北大学における人を対象とする医学系研究に関する倫理指針」に分類するⅢ種及びⅣ種に該当する研究【上記原則以外で所掌するもの】
- ヒトゲノム・遺伝子解析研究
なお、ヒトゲノム・遺伝子解析研究であっても、臨床研究倫理委員会の所掌するものに付随する研究である場合は、臨床研究倫理委員会において取扱う。 - ヒトiPS細胞又はヒト組織幹細胞からの生殖細胞の作成を行う研究であって、基礎的研究に係るもの
- ヒトES細胞を使用する研究であって、基礎的研究に係るもの
- 緊急倫理審査案件(患者対象を除く)
- 献体遺体使用の臨床医学教育・研究
- ヒトゲノム・遺伝子解析研究
-
病院臨床研究倫理委員会
【原則】
「東北大学における人を対象とする医学系研究に関する倫理指針」に分類するⅠ種及びⅡ種に該当する研究(主に東北大学病院で行われる研究)【上記原則以外で所掌するもの】
- 臨床研究推進センターシーズ
- 看護研究(東北大学病院看護部による研究)
東北大学倫理指針における研究分類
研究責任者は、「東北大学における人を対象とする医学系研究に関する倫理指針」における研究分類(下表)に基づいて、研究分類をご判断ください。
研究分類に関するフローチャートはこちらへ(倫理委員会ポータルサイト)
研究分類についてご不明な点は、上記「倫理委員会ポータルサイト」に専用の問い合わせフォームをご用意しておりますので、こちらからお問い合わせください。
| 研究分類 | 該当する研究 | 被験者 リスク |
社会的 リスク※ |
|---|---|---|---|
| 第Ⅰ種 |
該当する研究:
|
被験者リスク:高 | 社会的リスク:高 |
| 第Ⅱ種 |
該当する研究:
|
被験者リスク:低/中 | 社会的リスク:高 |
| 第Ⅲ種 |
該当する研究:
|
被験者リスク:低 | 社会的リスク:低 |
| 第Ⅳ種 |
該当する研究:
|
被験者リスク:低 | 社会的リスク:低 |
※社会的リスク:研究結果が医療現場の治療方針に与える影響の度合い等
倫理申請手順書・参考資料
手順書
本手順書を熟読のうえ申請願います。
人を対象とする医学系研究に
関する倫理申請手順書(
倫理委員会ポータルサイト)
参考資料
Ⅰ.学内規定等
- 国立大学法人東北大学における人を対象とする生命科学・医学系研究の実施に関する規程(PDF)
- 東北大学における人を対象とする医学系研究に関する倫理指針(倫理委員会ポータルサイト)
- 東北大学大学院医学系研究科倫理委員会内規(PDF)
- 東北大学大学院医学系研究科倫理委員会運営細則(PDF)
- 東北大学大学院医学系研究科ヒトiPS細胞又はヒト組織幹細胞からの生殖細胞の作成を行う研究に関する内規(PDF)
- 東北大学大学院医学系研究科ヒトES細胞の使用に関する内規(PDF)
Ⅱ.法律
臨床研究法の詳細は、厚生労働省のサイトにて最新の情報をご確認ください。
Ⅲ.その他指針等
- ヘルシンキ宣言(2013年10月WMAフォルタレザ総会で修正)(PDF)
- 人を対象とする生命科学・医学系研究に関する倫理指針(PDF)
- 人を対象とする生命科学・医学系研究に関する倫理指針ガイダンス(PDF)
- 人を対象とする医学系研究に関する倫理指針(平成29年2月28日一部改正)(PDF)
- 人を対象とする医学系研究に関する倫理指針ガイダンス(本編)(平成29年2月28日一部改訂)(PDF)
- 人を対象とする医学系研究に関する倫理指針ガイダンス(附則編)(PDF)
- 人を対象とする医学系研究に関する倫理指針ガイダンス(附則編)別添(経過措置に関するQ&A集)(PDF)
- Ethical Guidelines for Medical and Health
Research Involving Human Subjects(PDF) - 臨床研究に関する倫理指針(平成20年7月31日全部改正)(PDF)
- 臨床研究に関する倫理指針質疑応答集(Q&A)の改正について(医政研発第0612001号)(平成21年6月12日改正)(PDF)
- 疫学研究に関する倫理指針(平成25年4月1日一部改正)(PDF)
- 「疫学研究に関する倫理指針」についてのQ&A(平成19年11月1日)(PDF)
- ヒトゲノム・遺伝子解析研究に関する倫理指針(平成29年2月28日一部改正)(PDF)
- 「ヒトゲノム・遺伝子解析研究に関する倫理指針」についてのQ&A(平成29年4月19日改正)(PDF)
- ヒトiPS細胞又はヒト組織幹細胞からの生殖細胞の作成を行う研究に関する指針(PDF)
- 「臨床研究の利益相反ポリシー策定に関するガイドライン」
「21世紀型産学官連携手法の構築に係るモデルプログラム」(平成18年3月)(PDF)
各指針については、厚生労働省のサイトにて最新の情報をご確認ください。
関連リンク
- 医学系研究に関する倫理申請について(申請手順、倫理指針、内規など)
- 倫理委員会開催日、倫理申請講習会等
- 医学系研究に関する様式のダウンロード
- 倫理申請承認後の対応について(議事録掲載、臨床研究登録、進捗報告、英文承認書など)
- 各種指針に基づく情報公開について
問い合わせ先
※各連絡先アドレスの「*」を「@」に変換して送ってください。
医学系研究科倫理委員会に関する問い合わせ先
医学部・医学系研究科研究協力係:
med-kenkyo*grp.tohoku.ac.jp
病院臨床研究倫理委員会に関する問い合わせ先
病院研究協力係:
hosp-ken*grp.tohoku.ac.jp
臨床研究倫理委員会事務局:
ec*rinri.hosp.tohoku.ac.jp
研究分類、プロトコル作成支援に関する問い合わせ先
下記サイトの「お問い合わせ」フォームから「プロトコル相談」宛てにお問い合わせください
https://www.rinri.med.tohoku.ac.jp/portal/index.html
