医科学専攻
Developmental Neuroscience(United Centers for Advanced Research and Translational Medicine)発生発達神経科学(附属創生応用医学研究センター)
STAFF
Professor
-
Owada, YujiProfessor. 大和田 祐二 教授 (兼任)

Other Faculty / Staff
-
Kikkawa, Takako
Lect. 吉川 貴子 講師 -
Ochi, Shohei
Assistant Prof. 越智 翔平 助教 -
Sharmin, Naher
Assistant Prof. Sharmin Naher 助教 -
Jasper, Germeraad
Postdoc. Jasper Germeraad 学術研究員 -
Sara, Ebrahimi Azar
Postdoc. Sara Ebrahimi Azar 学術研究員
CONTACT
TEL:+81-22-717-8203
E-MAIL:
(「*」を「@」に変換してください)
OUTLINE
In order for the brain to perform higher functions, an appropriate number of neurons and Greer cells must be generated and positioned, and circuits must be formed correctly. Our laboratory aims to develop 1) molecular mechanisms of brain development and evolution, 2) genetic and epigenetic mechanisms of neurodevelopmental disorders, and 3) new behavioral analysis systems to understand sex and individual differences.We have clarified the mechanism by which the transcription factor Pax6 and its downstream molecules regulate neurogenesis in the cerebral cortex primordium. Recently, we have focused on the molecular mechanism by which mRNA of cyclin D2, which regulates the cell cycle, is transported to the basal tip of radial Greer cells and its effect on the development and evolution of the cerebral cortex.We have also modeled the effects of paternal aging on neurodevelopmental disorders reported in epidemiological studies in mice and identified epigenetic factors (DNA methylation, histone modification, and small RNA) that may be transmitted from sperm.Furthermore, we have developed IntelliCage, a workflow for automatic behavior analysis in group housing, and are promoting the introduction of AI analysis using big data to elucidate the correlation between behavioral differences between males and females and individual differences and biomarkers such as exosomes.
脳が高次機能を発揮するには、適切な数の神経細胞とグリアが生まれ、配置され、精緻な回路が形成される必要がある。私たちの研究室は、①脳の発生と進化の分子機構、②神経発達症の遺伝的・エピジェネティック基盤、③性差・個体差を捉える新規行動解析系の開発を柱とする。これまで転写因子Pax6と下流分子群が大脳皮質原基の神経新生を制御する仕組みを示し、現在はCyclin D2 mRNAが放射状グリアの基底端へ輸送される分子機構と、皮質発生・進化への寄与を追究している。疫学的に指摘される父加齢の影響をマウスでモデル化し、精子に由来するDNAメチル化・ヒストン修飾・小分子RNAなどの候補因子を同定した。さらに集団飼育下自動行動解析の研究用ワークフロー「IntelliProfiler」とAIによるビッグデータ解析を推進し、行動の雌雄差・個体差の指標とエクソソーム等のバイオマーカーとの関連を統合的に解明する。分子から回路、行動、そして社会実装へとつながる知を創出し、早期リスク評価や精密介入の基盤構築を目指す。
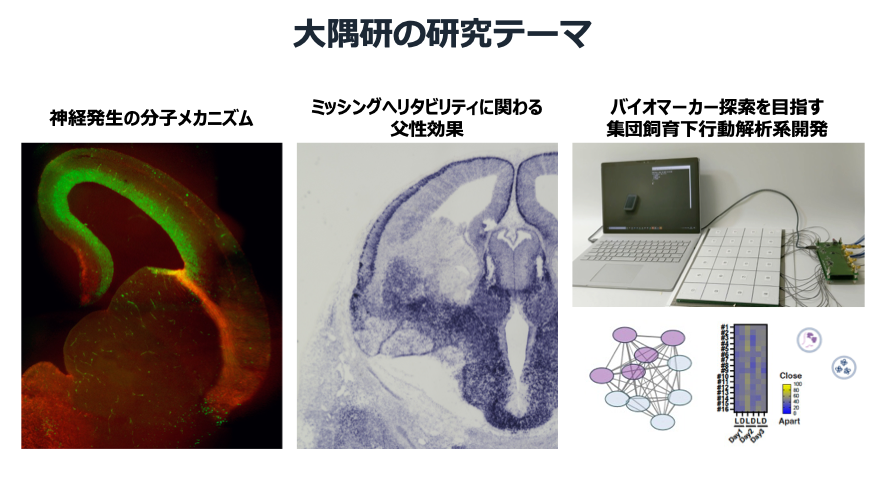
Current Research Themes at Osumi Lab
大隅研の現在の研究テーマ
Lab Members with Diverse Background
多様な研究室メンバー
Brain Development Lays All Aspects of Cognitive Function
脳の発生はすべての認知機能の源である
ARTICLE
Kasitipradit K, et al.: Sex-specific effects of prenatal bisphenol A exposure on transcriptome-interactome profiles of autism candidate genes in neural stem cells from offspring hippocampus. Sci Rep 2025, 15(1):2882. doi: 10.1038/s41598-025-86392-2.
Naher S, et al.: Kinesin-like motor protein KIF23 maintains neural stem and progenitor cell pools in the developing cortex. EMBO J 2025, 44(2):331-355. doi: 10.1038/s44318-024-00327-7. Epub 2024 Dec 4.
Miyahara K, et al.: Investigating the impact of paternal aging on murine sperm miRNA profiles and their potential link to autism spectrum disorder. Sci Rep. 2023. 13(1):20608. doi: 10.1038/s41598-023-47878-z.
Mai et al.: Advanced paternal age diversifies individual trajectories of vocalization patterns in neonatal mice. iScience 2022, 25(8):104834. doi: 10.1016/j.isci.2022.104834.
Yoshizaki K, et al.: Paternal age affects offspring via an epigenetic mechanism involving REST/NRSF. EMBO Rep 2021, 22(2):e51524. doi: 10.15252/embr.202051524.

 2025年度 医学部奨学賞・東北医学会奨学賞・医学部学生奨学賞授与式を行いました
2025年度 医学部奨学賞・東北医学会奨学賞・医学部学生奨学賞授与式を行いました
 小頭症を引き起こす新規原因分子を発見 胎仔脳の発生過程でのモーター分子の新たな機能
小頭症を引き起こす新規原因分子を発見 胎仔脳の発生過程でのモーター分子の新たな機能
 父親の加齢で精子の質が変化する 加齢マウス精子のマイクロRNA変化と次世代の神経発達障害リスク
父親の加齢で精子の質が変化する 加齢マウス精子のマイクロRNA変化と次世代の神経発達障害リスク
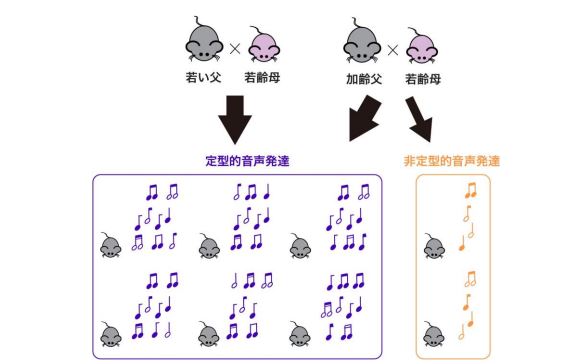 音声コミュニケーションの「個性」はどこから生まれるのか-父親の加齢が新生仔マウスの音声行動に及ぼす影響-
音声コミュニケーションの「個性」はどこから生まれるのか-父親の加齢が新生仔マウスの音声行動に及ぼす影響-